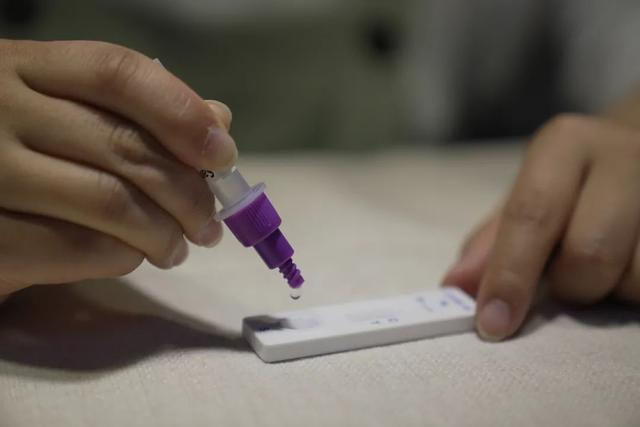
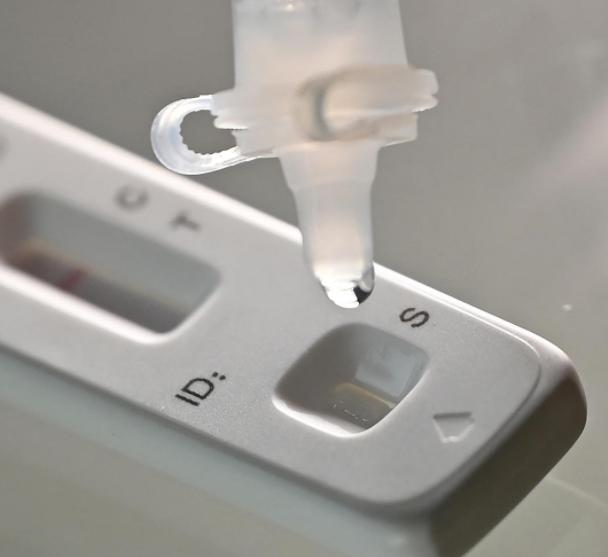
Den 12 marsth 2022, deNMPA (SFDA) utfärdat ett meddelande som godkänner ändringen av ansökan om självtest av COVID-19-antigenprodukter av Nanjing Vazyme BiotechCo., Ltd, Beijing Jinwofu Bioengineering TechnologyCo., Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd ochBeijing Savant Biotechnology Co., Ltd(Huaketai).Fem självtestande produkter för covid-19-antigen har lanserats.
Den 11 mars 2022 tillkännagav NHC att, för att ytterligare optimera teststrategin för nya coronaviruset och tillgodose behoven för förebyggande och kontroll av covid-19, beslutade det omfattande teamet för den gemensamma förebyggande och kontrollmekanismen i statsrådet att lägga till antigentestning till nukleinsyratestning och gjorde "ansökningsprotokollet för detektion av nya coronavirusantigen (försök)"
Protokollet specificerar den tillämpliga populationen för antigentestning:
Först, de som besöker primära medicinska institutioner och har symtom som luftvägar och feber inom 5 dagar efter symtomdebut;
För det andra, personal för karantänobservation, inklusive hemkarantänobservation, nära kontakt och undernära kontakt, observation av inträdeskarantän, personal inom inneslutningsområdet och kontrollområdet;
Den tredje är invånarna i samhället som har behov av antigen självdetektering.
Tips: Antigendetektering är ett viktigt komplement till nukleinsyradetektion, men resultaten av antigen självdetektering kan inte användas som grund för diagnos av infektion
Posttid: Mar-22-2022